GMP環境向けに設計。FDA 21 CFR Part 11に完全準拠し、監査証跡(Audit Trail)からプロセスバリデーションまで全工程の統計解析を支援します。
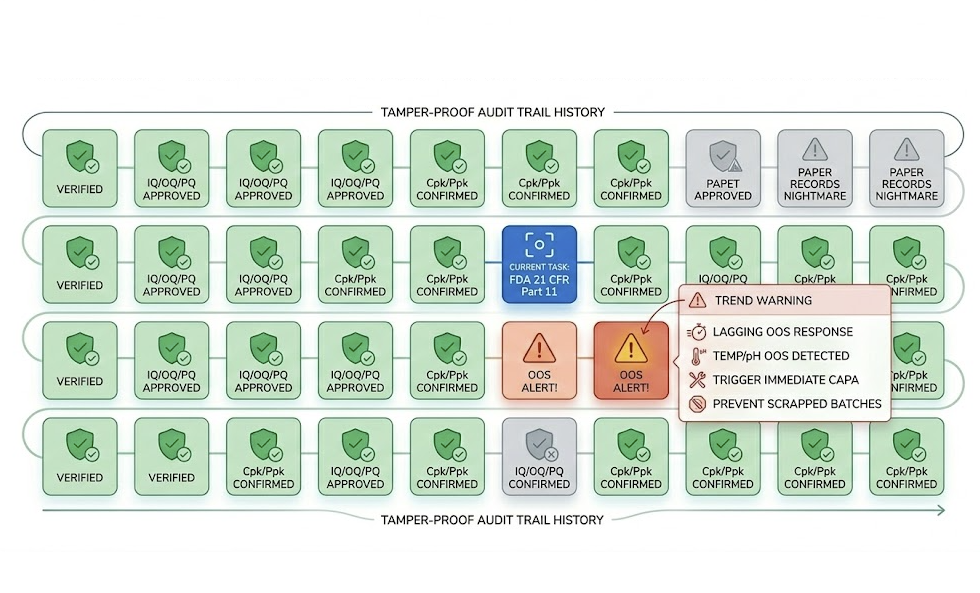
紙のBPR(製造指図記録書):書き損じ、記録の紛失、修正者の追跡不能……これらは監査における「致命傷」です。
IQ/OQ/PQ段階ではCpk/Ppkを証明するために大量のデータが必要です。Excelは非効率で改ざんされやすく、監査証跡もありません。
温度やpHがOOSになれば、即座にCAPA(是正予防措置)が必要です。リアルタイム警報がなければ、発見時には高価なバッチ全体が廃棄になる恐れがあります。
「データインテグリティ、バリデーション証拠、環境モニタリング、作業者の一貫性」を、その場しのぎの対応ではなく、システム本来の能力として定着させます。
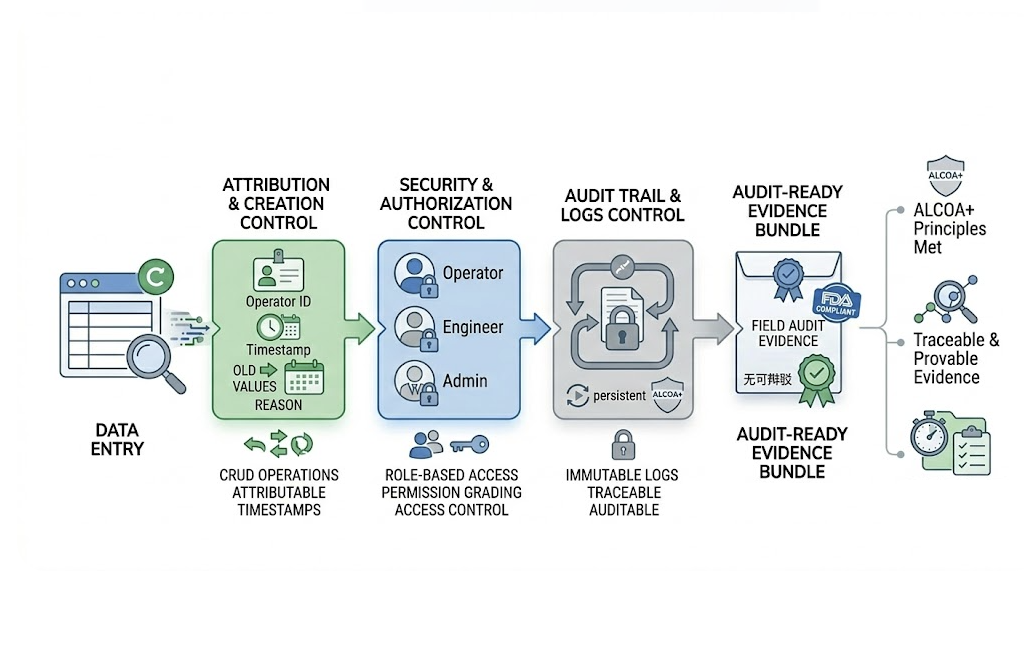
NEXSPC システムカーネル · セキュリティ&監査
すべてのデータ入力を、申し開きのできない「確実な証拠」にします。NEXSPCはアーキテクチャレベルで規制要件を厳守しています。
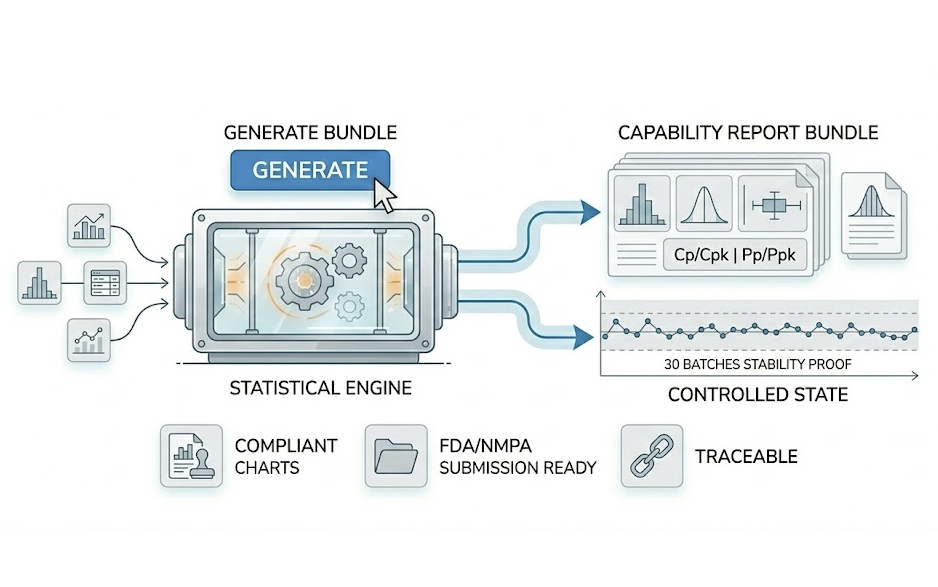
バリデーション (Validation)
データでプロセスが「堅牢(Robust)で信頼できる」ことを証明。PPQ段階では、申請と監査のために強力な統計的根拠が必要です。
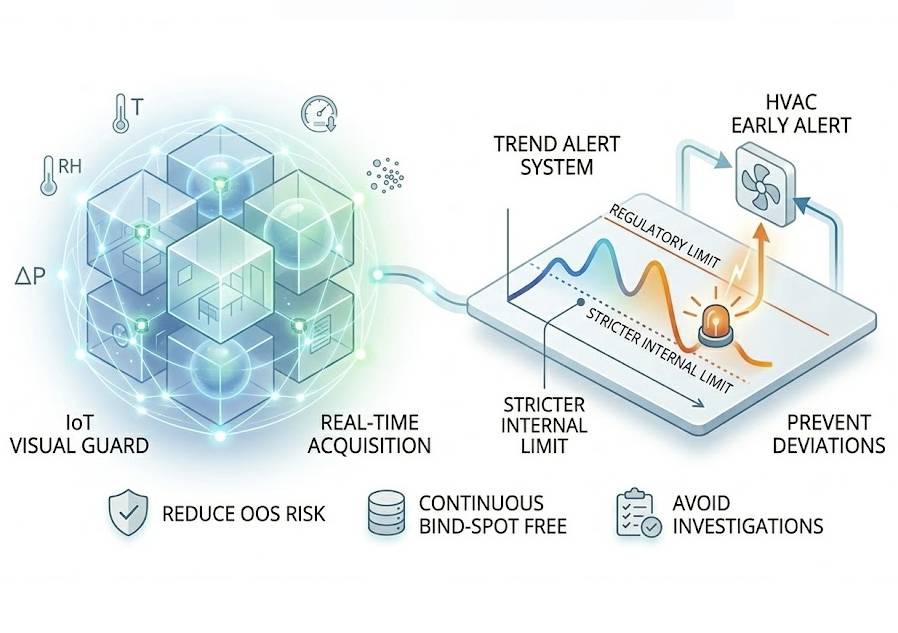
IoT EMS
すべての錠剤が適格な環境で製造されることを保証。GMPは温湿度、差圧(Differential Pressure)、微粒子の24時間365日の死角なき監視を厳格に求めています。
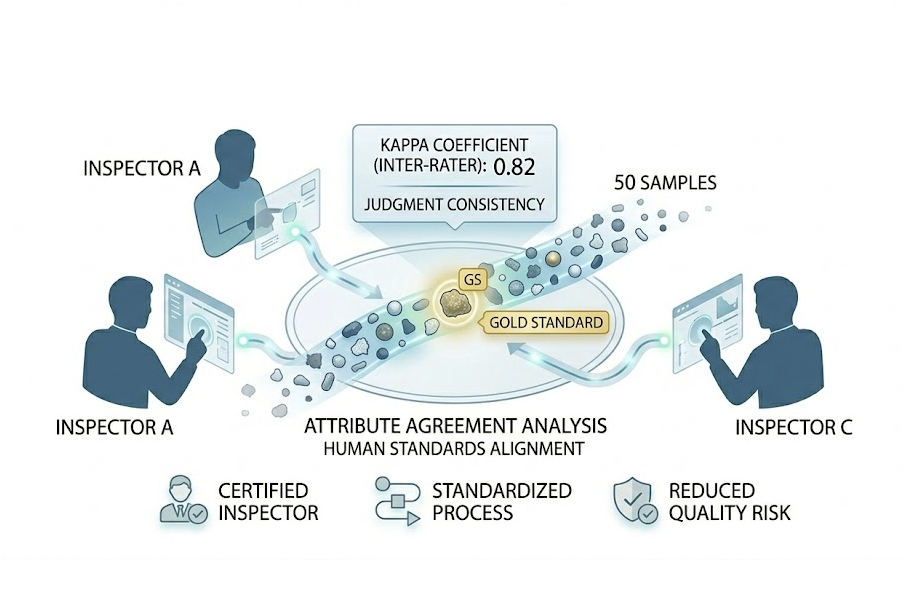
属性MSA (Attribute MSA)
目視判定基準を統一し、見逃し(False Negative)と過剰検出(False Positive)を削減。異物検査などの人的工程には、統計的な整合性評価が不可欠です。
コンプライアンスを「形式」から「システム化された証拠連鎖」へ変革し、監査と申請を確実にします。
| 次元(Dimension) | 従来のExcel / 紙運用 | NEXSPC 医薬コンプライアンス版 |
|---|---|---|
| データインテグリティ | 紙は破損・紛失のリスク。Excelは痕跡なく改ざん可能。 | 全工程の監査証跡(Audit Trail)、ALCOA+原則に準拠。 |
| OOS(規格外)管理 | OOS発生後に逸脱(Deviation)票を手書き。対応が遅れる。 | OOS即時アラーム。システムがイベント時間を自動記録。 |
| バリデーション効率 | 検証データの整理に数週間。人為的ミスのリスク大。 | 検証バッチデータの自動集計。ワンクリックでレポート出力。 |
| 環境モニタリング | 定時的な巡回記録。データの空白期間(Gaps)が存在。 | センサーによる24時間連続収集。死角なし。 |
ソリューションについてはご理解いただけましたか?準備はいいですか?右側のボタンをクリックして、料金プランを確認するか、今すぐご相談ください。