專為 GMP 環境設計。完全符合 FDA 21 CFR Part 11 要求,提供從審計追踪到工藝驗證 (Process Validation) 的全流程統計支持。
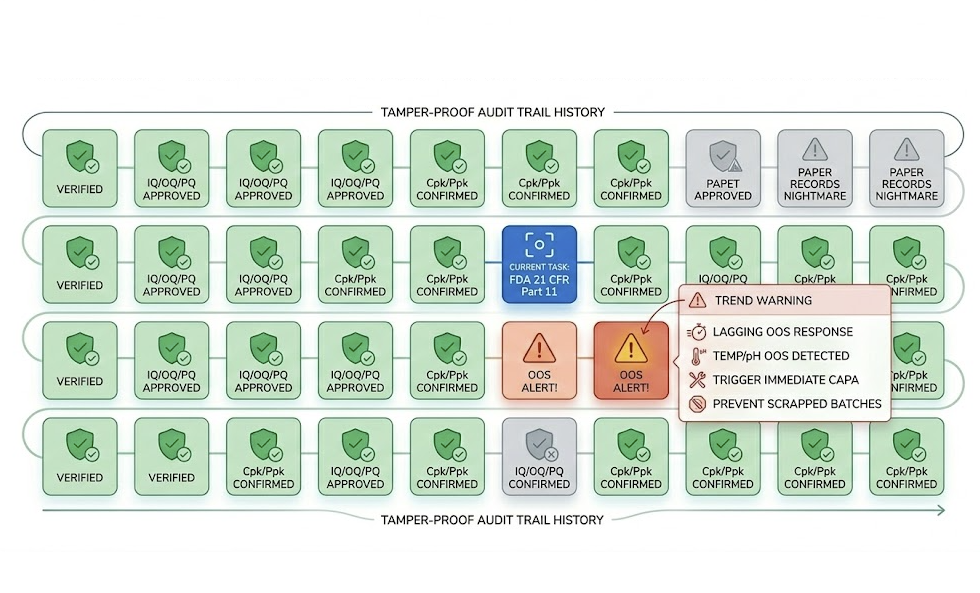
紙筆記錄 BPR:筆誤修改、記錄丟失、無法追溯修改人……這些都是審計中的「致命傷」。
IQ/OQ/PQ 階段需要大量數據證明 Cpk/Ppk。用 Excel 做報告效率低,且文件易被修改,缺乏審計追踪。
溫度、pH 一旦 OOS 必須立即啟動 CAPA。若不能實時報警,等發現時整批昂貴藥液可能已報廢。
讓「數據完整性、驗證證據、環境監控、人員一致性」變成系統能力,而不是臨時應付。
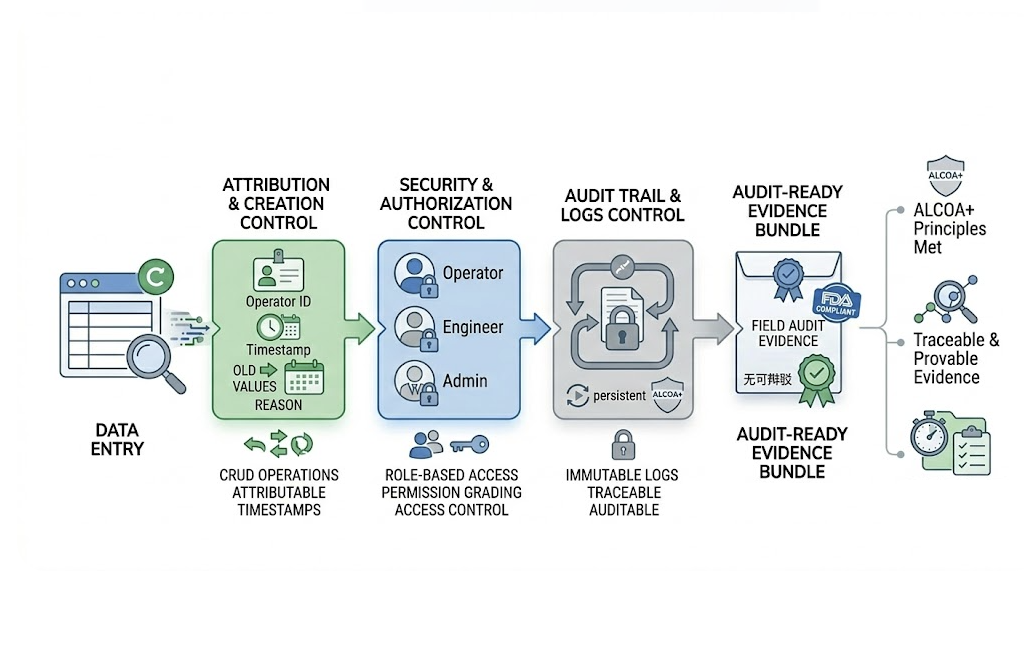
NEXSPC 系統內核 · 安全與審計
讓每一次數據錄入都成為不可抵賴的「呈堂證供」。NEXSPC 在底層架構上嚴格遵循法規要求。
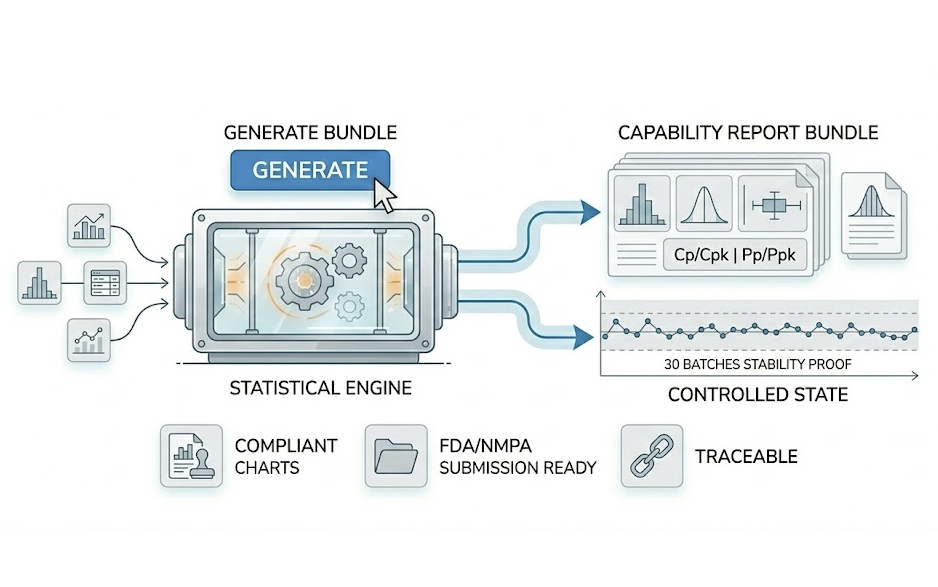
Validation
用數據證明工藝「穩健可靠」。在 PPQ 等驗證階段,需要強有力的統計證據支持申報與審計。
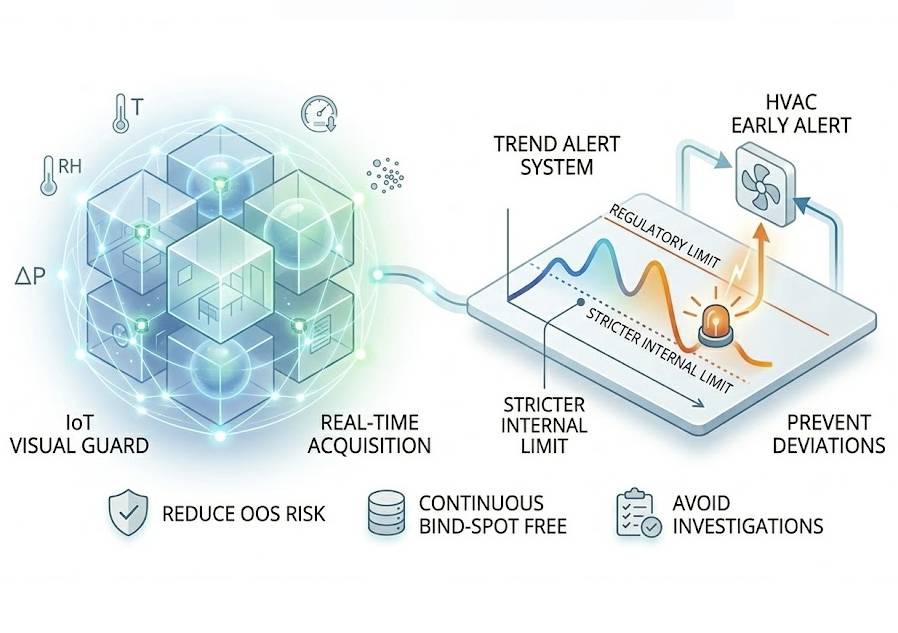
IoT EMS
確保每一粒藥片都在合格環境中誕生。GMP 對温濕度、壓差、塵埃粒子要求極其嚴格,必須 24/7 無盲區。
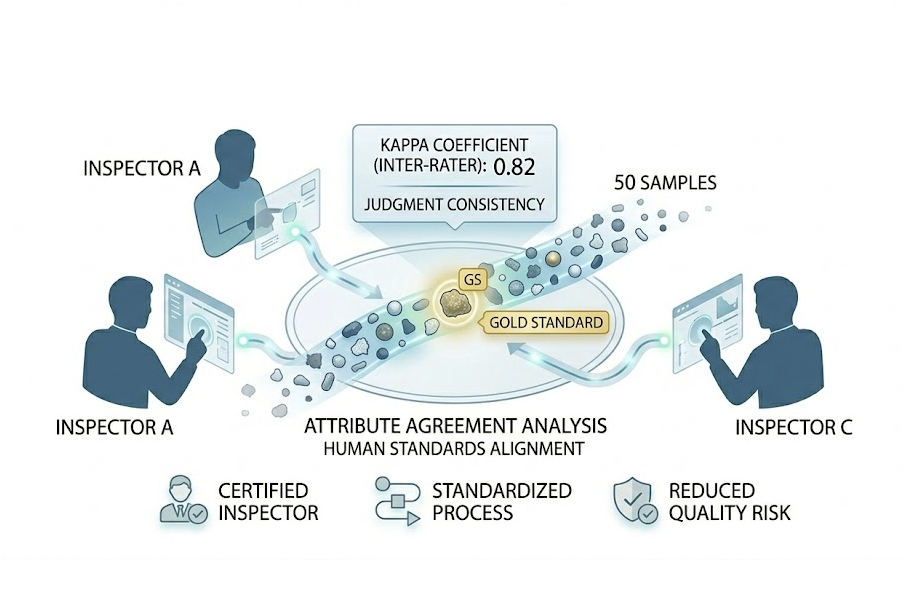
Attribute MSA
統一人眼判定標準,減少漏檢與誤殺。燈檢(異物檢查)是典型依靠人工的工序,需要用統計量衡量一致性。
把合規從「形式」變成「系統證據鏈」,審計與申報都更穩。
| 維度 | 傳統 Excel / 紙質模式 | NEXSPC 醫藥合規版 |
|---|---|---|
| 數據完整性 | 紙張易破損/丟失,Excel 易被篡改無痕跡 | 全流程審計追踪,滿足 ALCOA+ 原則 |
| OOS 管理 | 超標後人工填寫偏差單,流程慢 | OOS 觸發即時報警,系統自動記錄事件時間 |
| 驗證效率 | 驗證數據需人工整理數週,容易出錯 | 驗證批次數據自動聚合,一鍵導出驗證報告 |
| 環境監控 | 人工定時巡檢抄表,有數據空窗期 | 傳感器 24 小時連續採集,無盲區 |
了解了我們的解決方案,您準備好了嗎?點擊右方按鈕,查看定價計劃或立即咨詢