Dirancang untuk lingkungan GMP. Sepenuhnya mematuhi FDA 21 CFR Part 11, menawarkan dukungan statistik dari Jejak Audit hingga Validasi Proses.
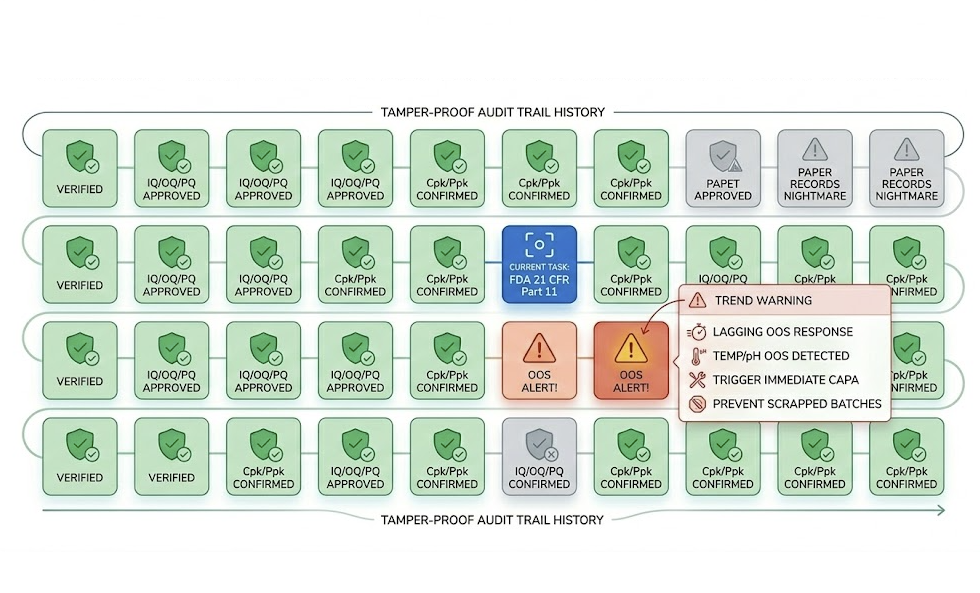
BPR Kertas: Kesalahan pena, catatan hilang, edit tak terlacak... Ini adalah 'luka fatal' dalam audit.
Tahap IQ/OQ/PQ butuh data Cpk/Ppk masif. Excel tidak efisien, mudah diubah, dan tanpa Jejak Audit.
Suhu/pH OOS butuh CAPA segera. Tanpa alarm real-time, batch mahal bisa terbuang.
Jadikan 'Integritas Data, Bukti Validasi, Pemantauan Lingkungan, Konsistensi Personel' sebagai kemampuan sistem, bukan perbaikan sementara.
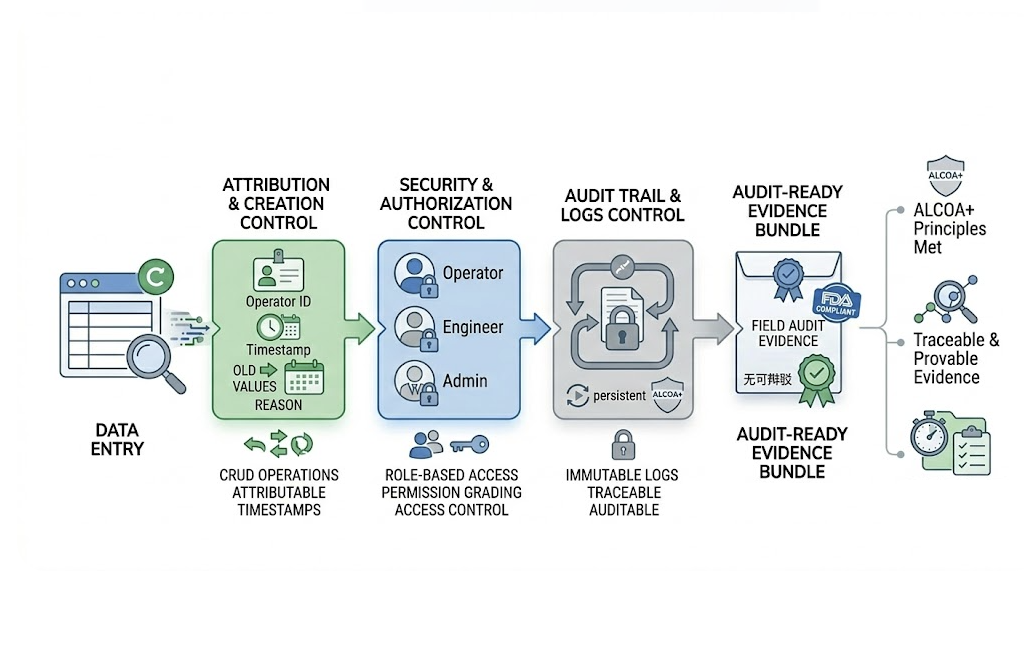
Kernel Sistem NEXSPC · Keamanan & Audit
Jadikan setiap entri data sebagai 'bukti tak terbantahkan'. NEXSPC mematuhi peraturan secara ketat pada tingkat arsitektur.
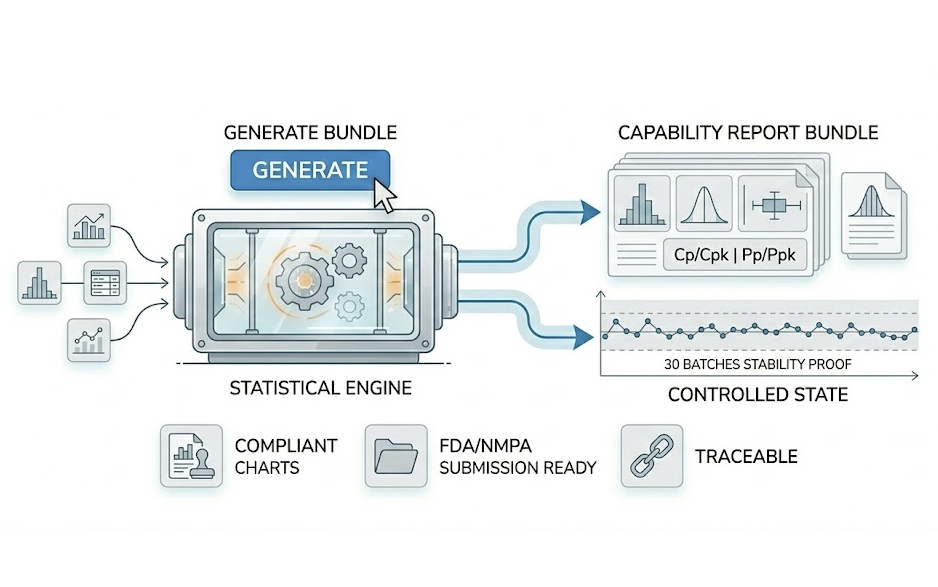
Validasi
Buktikan proses 'kuat dan andal'. Tahap PPQ butuh bukti statistik kuat untuk pengajuan dan audit.
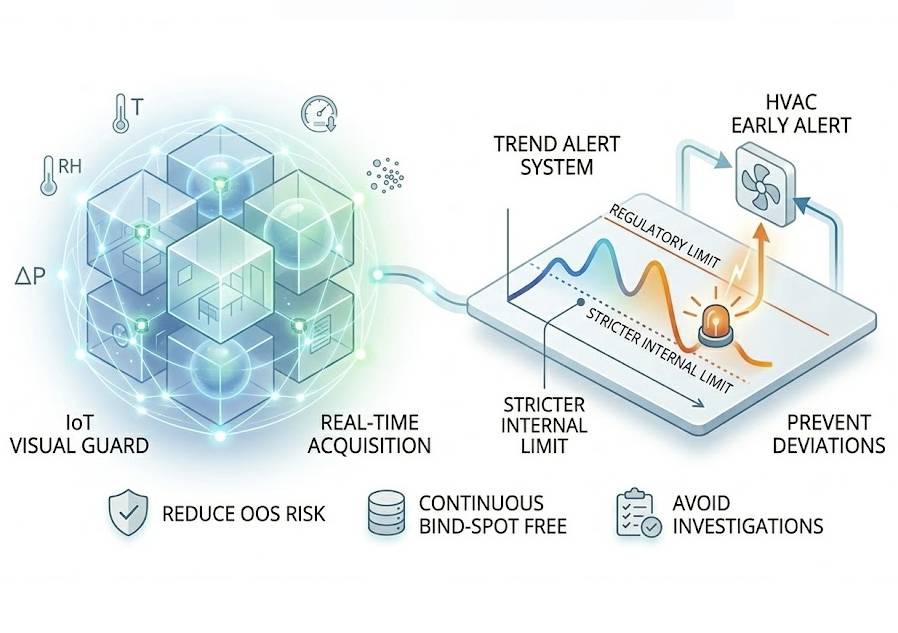
IoT EMS
Pastikan setiap pil diproduksi di lingkungan yang memenuhi syarat. GMP mewajibkan pemantauan ketat Suhu/RH, Tekanan Diferensial, dan Partikel 24/7.
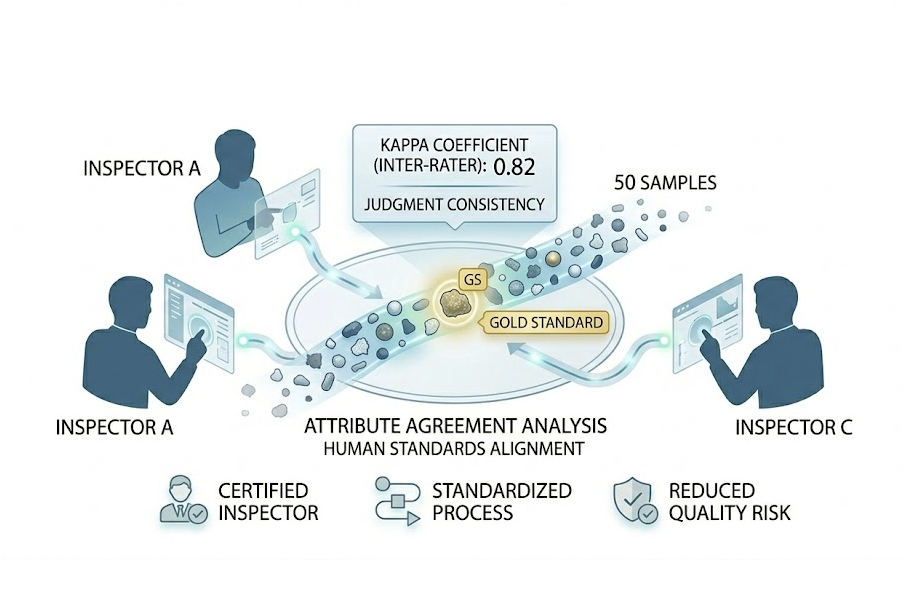
MSA Atribut
Satukan standar penilaian manusia, kurangi negatif palsu & positif palsu. Inspeksi visual manual butuh statistik.
Ubah kepatuhan dari 'formalitas' menjadi 'rantai bukti sistematis', memastikan stabilitas audit.
| Dimensi | Mode Excel / Kertas Tradisional | NEXSPC Edisi Kepatuhan Farmasi |
|---|---|---|
| Integritas Data | Kertas sobek/hilang; Excel dimodifikasi tanpa jejak. | Jejak Audit Penuh, memenuhi prinsip ALCOA+. |
| Manajemen OOS | Formulir deviasi manual setelah OOS; proses lambat. | Alarm OOS instan; sistem mencatat waktu kejadian. |
| Efisiensi Validasi | Berminggu-minggu kompilasi data manual; rawan kesalahan. | Agregasi otomatis data batch; laporan validasi satu klik. |
| Pemantauan Lingkungan | Patroli terjadwal manual; ada kesenjangan data. | Sensor mengumpulkan terus menerus 24/7; tanpa titik buta. |
Sudah memahami solusi kami, apakah Anda siap? Klik tombol di kanan untuk Lihat Harga atau Konsultasi Sekarang.